-
Numero contenuti
24969 -
Iscritto
-
Ultima visita
Tipo di contenuto
Profili
Forum
Orchidee
Diventa Socio
Calendario
Messaggi pubblicati da Tomaso Lezzi
-
-
Boletopsis grisea (Peck) Bondartsev & Singer; Roma, Castel Fusano; Foto di Tomaso Lezzi
Ritrovamento sotto Pinus pinea e Quercus ilex, il sapore rilevato è amaro, verificata la macroreazione sulla carne che diventa verde con NaOH (base forte).
In Italia sono presenti due specie di Boletopsis molto simili:
Boletopsis grisea (Peck) Bondartsev & Singer, caratterizzata da:
- Crescita preferenziale sotto Pinus pinea.
- Carne decisamente amara.
- Reazione verde alle base forti.
Boletopsis leucomelaena (Pers.) Fayod, caratterizzata da:
- Crescita preferenziale sotto Abeti.
- Carne non particolarmente amara.
- Reazione immediata al nero con le basi forti.
- Crescita preferenziale sotto Pinus pinea.
-
-
Russula fragilis (Pers.: Fr.) Fr,; Roma, Castel Fusano; Foto di Tomaso Lezzi
Russula fragilis è veramente "fragile" e le lamelle si rompono molto facilmente durante la manipolazione.
Il gambo cavo, le lamelle seghettate sul filo, l'odore di cocco e il sapore decisamente piccante sono altre caratteristiche che ci aiutano a determinarla correttamente.
Particolare delle lamelle seghettate.
-
Ciao Esakki, sporata bruna, gambo leggermente fioccoso, soprattuto nella parte alta, direi che ci troviamo nel genere Hebeloma.

Tom

-
Apro il post di Dicembre per i nuovi contributi natalizi

Tom

-
-
Ciao Glacial, ci sono due soli generi che hanno la carne cassante, cioè non fibrosa, ma fatta da cellule sferiche, come se fossero pallini di polistirolo. Questa caratteristica microscopica si riflette in alcune proprietà macroscopiche, come il fatto che la carne si rompa di netto come succede per un gessetto delle lavagne.
I due generi sono: Russula, che alla frattura non emette latice; e Lactarius, che come dice il nome all rottura secerne latice, quindi siamo nel genere Lactarius.
Per arrivare a determinare le specie in questo genere è importante che controlli di che colore è il latice alla fuoriuscita, se c'è un viraggio del colore del latice dopo un po' di tempo e il sapore del latice stesso, se dolce o piccante, e infine l'odore quando strofini le lamelle.
Quando incominci a riconoscere i generi principali sarà più facile sapere quali sono le cose da controllare per procedere nella determinazione.

Tom

-
Ciao Glacial, Per quanto riguarda la commestibilità delle Ramaria il mio consiglio è di fotografarle e lasciarle nel bosco

Alcune specie tossiche con colori rosati come Ramaria formosa sono molto difficilmente riconoscibili quando sono mature, perché tutte le Ramaria producono spore di colore ocra che rivestono col tempo i rami e che a maturità rendono tutte le specie di questo genere più o meno dello stesso colore.
La Ramaria formosa di cui trovi qui il collegamento alla scheda in archivio, da una sindrome gastrointestinale piuttosto importante, persone che l'hanno mangiata per sbaglio pensando che fosse una delle manine commestibili... non hanno fato a tempo ad arrivare in bagno...

 :D
:DCi sono tanti funghi più buoni e più sicuri, il mio consiglio è di evitare il consumo delle Ramaria.
Tom

-
ciao Glacial, quando i funghi sono vecchi non si conserva né il cappello, né il gambo; ti mangeresti la mezza bistecca di sinistra, se la parte di destra è andata a male?

Attenzione perché una buona parte delle intossicazioni da funghi non sono dovute a specie tossiche, ma a specie (ex-commestibili) avariate!!!

Tom

-
ciao Glacial, ti confermo Amanita muscaria, per le foto meglio queste fatte in habitat, piuttosto che le altre sul tavolo di cucina!

Cerca sempre di fotografare le specie che trovi nel loro ambiente, oltre a risultarne delle foto più belle, darai maggiori informazioni a chi ti aiuta nelle determinazioni delle specie proposte

Tom

-
Ciao Glacial, sì, Gyroporus castaneus, ricordati che i binomi latini usati per i nomi dei funghi, delle piante e degli animali sono appunto dei Binomi! Se dici solo "castaneus", oltre a non essere corretto come terminjlogia, molte persone faranno fatica a capire di cosa stai parlando

Tom

-
Ciao Glacial,
Colpito e affondato: Clitocybe odora!
Tom

-
No, è il suo colore!

Anche Clavulina cinerea, come dice il nome, ha più o meno lo stesso colore grigiastro
Tom

-
-
Lepiota lilacea Bresadola, Roma, Villa Pamphili, Foto di Tomaso Lezzi
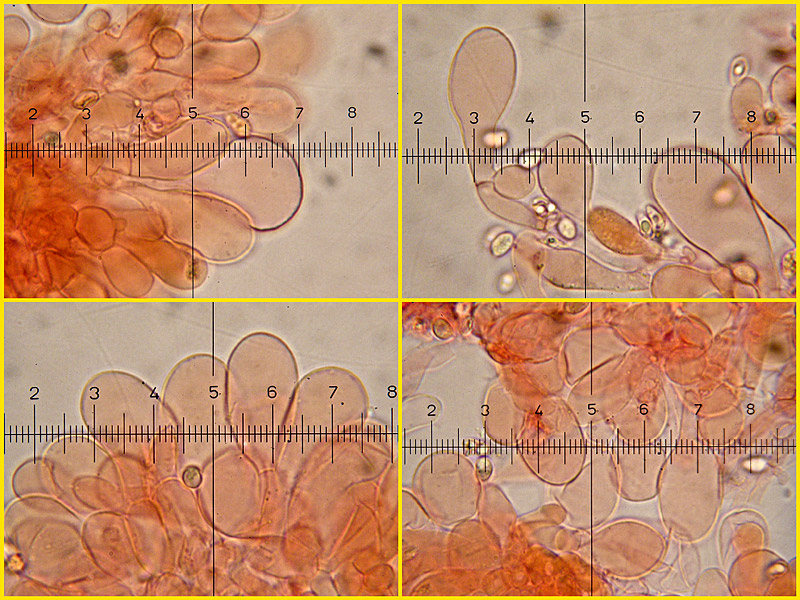
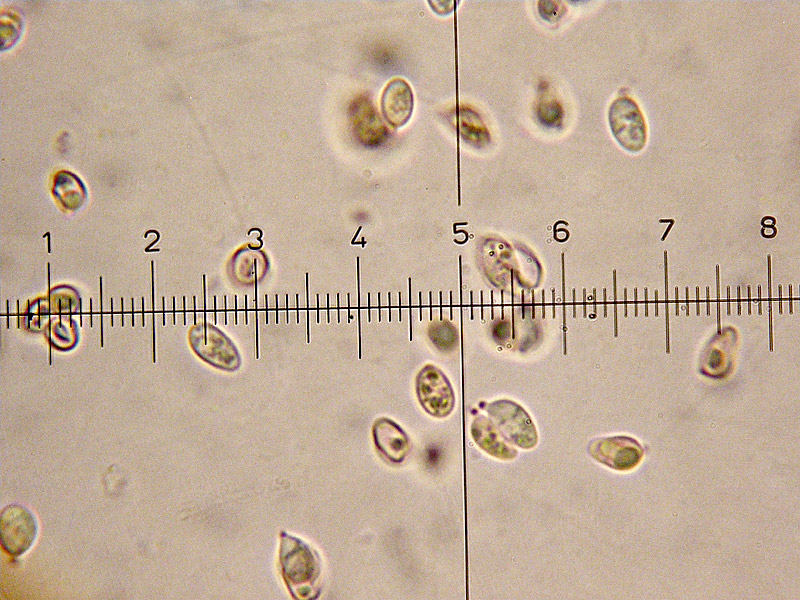
Lepiota caratterizzata dal cappello con zona discale ben definita e squame scure su fondo chiaro, gambo con un anello ben definito, con la faccia inferiore scura, concolore alle squame del cappello; odore simile a quello di Lepiota cristata, più leggero e aromatico. Microscopicamente presentra la cuticola con un imenoderma di cellule clavate; cheilocistidi clavati; spore ellissoidali, piccole, misure rilevate: 4,5-5,8 × 2,6-3,3 µm; Qm = 1,7.
Particolare dell'anello con la faccia inferiore scura, concolore alle squame del cappello.
-
Indice Regione Abruzzo, mese di Novembre 2011, totale n° 7 specie.
-
Amanita muscaria (L.) Lam., Post #2,
-
Coprinus comatus (Müll.: Fr.) Pers., Post #3
-
Cortinarius infractus f. olivellusM.M. Moser, Post #9
-
Inonotus tamaricis (Pat.) Maire, Post #7
-
Psathyrella lacrymabunda (Bull.: Fr.) Moser, Post #4,5
-
Tricholoma equestre var. populinumMort. Chr. & Noordel.
= Tricholoma frondosae Kalamees & Shchukin, Post #6
-
Tricholoma populinum Lange, Post #8
Tom

-
Amanita muscaria (L.) Lam., Post #2,
-
Dobbiamo sempre ricordarci che in generale un esame microscopico da solo di solito serve a poco, se non è sempre accompagnato da precise osservazioni macro, odore, sapore, eventuali viraggi, ecc. Caratteri che vanno sempre osservati sui campioni freschi.
In questo caso dopo le osservazioni macro, che ti portano facilmente al genere, devi passare ai caratteri micro per distinguere le specie.

Tom

-
Indice Regione Lazio, mese di Dicembre 2011, totale n° 49 specie (nella lista seguente sono comprese anche alcune sinonimie).
-
Abortiporus biennis (Bull.) Singer; ; Post #19
-
Agaricus freirei Blanco-Dios; Post #77, 78, 79, 80; Microscopia #81, 82, 83, 84, 85
-
Amanita citrina (Schaeffer) Persoon; Post #53
-
Amanita gracilior Bas & Honrubia; Post #31, 35
-
Amanita ovoidea (Bull.) Link; Post #52
-
Amanita rubescens (Pers.: Fr) S.F.Gray; Post #21
-
Bolbitius vitellinus (Pers.) Fr.; Post #38,
-
Boletopsis grisea (Peck) Bondartsev & Singer; Post #5
-
Callistosporium xanthophyllum (Malençon & Bertault) Bon; Post #26
-
Chroogomphus rutilus (Fr.) Massee; Post #49
-
Collybia butyracea (Bull.: Fr.) Kummer; Post #4; 10, 11
-
Coprinellus domesticus (Bolton) Vilgalys, Hopple & Jacq. Johnson = Coprinus domesticus (Bolt.: Fr.) Gray; Post #70; Microscopia #71, 72, 73, 74
-
Coprinus domesticus (Bolt.: Fr.) Gray = Coprinellus domesticus (Bolton) Vilgalys, Hopple & Jacq. Johnson; Post #70; Microscopia #71, 72, 73, 74
-
Cortinarius rufo-olivaceus (Pers.) Fr.; Post #65; Microscopia #66
-
Cortinarius subturibulosus var. bombycinus (Mahiques & Burguete) Suár.-Sant. & A. Ortega; Post #91; Microscopia #92, 93
-
Crucibulum laeve (Bull.) Kambly; Post #50
-
Daldinia concentrica (Bolton) Ces. & De Not.; Post #75
-
Entoloma bloxamii (Berk.) Sacc.; Post #24
-
Entoloma chalybaeum (Pers.) Noordel.; Post #89; Microscopia #90
-
Galerina laevis (Pers.) Singer; Post #32; Microscopia #33, 34
-
Gymnopilus spectabilis (Wein.: Fr.) A.H. Smith; Post #20
-
Gyroporus castaneus (Bull.: Fr.) Quél.; Post #43
-
Hygrocybe persistens var. persistens (Britzelmayr) Singer; Post #25
-
Hygrophorus russula (Schaeff.) Kauffman; Post #22, 68
-
Hypholoma rubrococcineum (Balletto) Nonis = Nematoloma rubrococcineum Balletto= Psilocybe ceres (Cooke & Massee) Sacc. = Leratiomyces ceres (Cooke & Massee) Spooner & Bridge; Post #55, 56, 57; Microscopia #58
-
Inocybe godeyi Gillet; Post #23
-
Lactarius chrysorrheus Fr.; Post #46
-
Lactarius luridus (Pers.: Fr.) Gray Post #86; Microscopia #87
-
Leccinum lepidum (Bouchet ex Essette) Quadraccia; Post #27, 54, 67
-
Lepiota aspera (Pers.: Fr.) Quél.; Post #12, 13, 14, 15, 17; Microscopia #16
-
Lepiota cristata (Bolt.: Fr.) Kummer; Post #9; Microscopia #69
-
Lepiota rhodorrhiza Romagn. & Locq. ex Orton; Post #36
-
Leratiomyces ceres (Cooke & Massee) Spooner & Bridge = Psilocybe ceres (Cooke & Massee) Sacc. = Nematoloma rubrococcineum Balletto = Hypholoma rubrococcineum (Balletto) Nonis; Post #55, 56, 57; Microscopia #58
-
Lyophyllum decastes (Fr.: Fr.) Sing.; Post #39, 40; Microscopia #61
-
Melanoleuca exscissa (Fr.); Post #62; Microscopia #63, 64
-
Mycena seynii Quélet; Post #6
-
Nematoloma rubrococcineum Balletto = Psilocybe ceres (Cooke & Massee) Sacc. = Leratiomyces ceres (Cooke & Massee) Spooner & Bridge = Hypholoma rubrococcineum (Balletto) Nonis; Post #55, 56, 57; Microscopia #58
-
Ossicaulis lignatilis (Pers.) Redhead & Ginns = Pleurocybella lignatilis (Pers.) Singer = Pleurotus lignatilis (Pers.) P. Kumm.; Post #8, 44
-
Phellodon niger (Fr.) P. Karst.; Post #51
-
Pleurocybella lignatilis (Pers.) Singer = Ossicaulis lignatilis (Pers.) Redhead & Ginns = Pleurotus lignatilis (Pers.) P. Kumm.; Post #8, 44
-
Pleurotus lignatilis (Pers.) P. Kumm. = Pleurocybella lignatilis (Pers.) Singer = Ossicaulis lignatilis (Pers.) Redhead & Ginns; Post #8, 44
-
Psathyrella conopilus (Fr.) A. Pearson & Dennis; Post #76
-
Psilocybe ceres (Cooke & Massee) Sacc. = Leratiomyces ceres (Cooke & Massee) Spooner & Bridge = Nematoloma rubrococcineum Balletto = Hypholoma rubrococcineum (Balletto) Nonis; Post #55, 56, 57; Microscopia #5
-
Ramaria bourdotiana Maire; Post #87; Microscopia #88, 89
-
Russula cyanoxantha (Schaeff.) Fr.; Post #41
-
Russula fragilis (Pers.: Fr.) Fr.; Post #2, 3, 59
-
Russula graveolens fo. cicatricata P.-J. Keizer & Arnolds; Post #28
-
Russula heterophylla Fr.; Post #42
-
Russula persicina Krombholz; Post #7
-
Russula torulosa Bresadola; Post #48
-
Sphaerobolus stellatus Tode; Post #29, 30
-
Trichaptum biforme (Fr.) Ryvarden; Post #60
-
Tricholoma pseudoalbum Bon; Post #45
-
Tricholoma scalpturatum (Fr.) Quélet,; Post #47
-
Volvariella gloiocephala (De Cand.: Fr.) Boek. & End, = Volvopluteus gloiocephalus (DC.: Fr.) Vizzini, Contu & Justo; Post #18, 37
-
Volvopluteus gloiocephalus (DC.: Fr.) Vizzini, Contu & Justo = Volvariella gloiocephala (De Cand.: Fr.) Boek. & End; Post #18, 37
Tom

-
Abortiporus biennis (Bull.) Singer; ; Post #19
-
Nicola sei più informato di Wikipedia!
 :D
:D 
Tom

-
Ciao Massimo, concordo con Claudio e punto 5 centesimi (di più proprio non si può!) su Psathyrella sp. per quello centrale

Tom

-
-
Sul gruppo degli Xanthodermatei l'odore è più forte e meglio percepibile alla base del gambo, proprio dove diventa giallo cromo, alla sezione. Se gratti o stropicci questa parte è più facilmente percepibile, per gli odori i funghi vanno un po' "ciancicati"!

Per riportare alla mente un odore più conosciuto, visto che non tutti conoscono il Fenolo, puoi pensare all'odore dell'inchiostro delle vecchie penne stilografiche (i più giovani non conosceranno neanche questo di odore!)

Tom

-
Concordo con chi mi ha preceduto e aggiungo un'altra possibilità che puoi verificare: Clitocybe alkaliviolascens, che come dice il nome si colora vinoso-viola se mettiamo una goccia di NaOH oppure KOH (alcali) sul cappello.
Tom

-
Ciao Venturino,
I caratteri che ti aiutano a riconoscerla sono: verruche abbastanza piccole, bianche; margine rigato; anello alto; volva alla base circoncisa (con confine tagliato abbastanza nettamente) a forma di "cipolletta".

Tom

PS Concordo che le specie tossiche è meglio evitare di assaggiarle













2011.12 - Lazio - Tutor Tomaso Lezzi
in Funghi trovati Anno 2011
Inviato
Mycena seynii Quélet; Roma, Castel Fusano; Foto di Tomaso Lezzi
Questa specie di Mycena cresce tipicamente su pigne di Pino.